Рефераты по коммуникации и связи
Рефераты по косметологии
Рефераты по криминалистике
Рефераты по криминологии
Рефераты по науке и технике
Рефераты по кулинарии
Рефераты по культурологии
Рефераты по зарубежной литературе
Рефераты по логике
Рефераты по логистике
Рефераты по маркетингу
Рефераты по международному публичному праву
Рефераты по международному частному праву
Рефераты по международным отношениям
Рефераты по культуре и искусству
Рефераты по менеджменту
Рефераты по металлургии
Рефераты по налогообложению
Рефераты по оккультизму и уфологии
Рефераты по педагогике
Рефераты по политологии
Рефераты по праву
Биографии
Рефераты по предпринимательству
Рефераты по психологии
Рефераты по радиоэлектронике
Рефераты по риторике
Рефераты по социологии
Рефераты по статистике
Рефераты по страхованию
Рефераты по строительству
Рефераты по схемотехнике
Рефераты по таможенной системе
Сочинения по литературе и русскому языку
Рефераты по теории государства и права
Рефераты по теории организации
Рефераты по теплотехнике
Рефераты по технологии
Рефераты по товароведению
Рефераты по транспорту
Рефераты по трудовому праву
Рефераты по туризму
Рефераты по уголовному праву и процессу
Рефераты по управлению
Лабораторная работа: Визначення теплоти розчинення і гідратації солі
Лабораторная работа: Визначення теплоти розчинення і гідратації солі
Лабораторна робота № 1. „Визначення теплоти розчинення і гідратації солі”
Мета роботи:
1. Познайомитись з калориметричним методом вимірювання теплових ефектів.
2. Визначити теплоти розчинення безводного купрум (II) сульфату мідного купоросу.
3. Визначити теплоту утворення кристалогідрату СuSО4•5Н2О з безводної солі.
На занятті необхідно:
1. Виконати роботу у відповідності до вимог даної методично розробки.
2. Навчитись користуватись калориметром та визначати його теплоємність.
3. Розрахувати теплоту розчинення солі та теплоту гідратації.
4. Оформити звіт про виконану роботу і здати його викладачу.
Перелік обладнання та реактивів:
1. Калориметр;
2. термометр;
3. технохімічні ваги;
4. пробірки (3 шт.);
5. секундомір;
6. порцелянова ступка;
7. KNO3
8. СuSО4, СuSО4•5Н2О
Порядок виконання роботи:
Дослід 1. Визначення сталої калориметра
1. Суху пробірку попередньо зважити на технохімічних терезах.
2. Ретельно розтерти калій нітрат в порцеляновій ступці і засипати його у зважену пробірку приблизно на ¼ її висоти.
3. Зважити на технохімічних терезах пробірку з сіллю (з точністю до 0,01г). За різницею зважувань знайти масу солі, що повинна знаходитись в межах 4 -7 г. Отримані дані занести в таблицю 1.
4. У стакан калориметра налити 250 мл води, закрити калориметр кришкою і встановити в менший її отвір термометр, а в більший– пробірку з сіллю. (Для того щоб пробірка не провалювалась в калориметр на не потрібно надіти гумове кільце!).
5. Вимірювання провести в три етапи (періоди): попередній, головний заключний.
6. Ввімкнути калориметр в мережу змінного струму, потім ввімкнути тумблером мішалку, а через 1-2 хвилини– секундомір.
7. Попередній етап: вимірювання температури провести з точністю до 0,5°С через кожні 30 сек. протягом 5 хв.
8. Головний етап: не виключаючи секундоміра роз бити пробірку з сіллю так, щоб вся сіль висипалась у воду. Якщо температура змінюється дуже швидко, реєструвати її з меншою точністю.
9. Заключний етап: іще провести вимірювання температури через кожн 30 сек. протягом 5 хв. до встановлення рівномірного ходу температури (теж з точністю до 0,5°С).
10.Дані всіх вимірювань занести в таблицю 2.
11.Для розрахунку точно зміни температури на міліметровому папері побудувати графік, відкладаючи по вісі абсцис час, а по вісі ординат– зміну температури (масштаб на абсцисі- 1хв: 1см, а на ординаті– 1°К: 5см). З’єднані точки дадуть дві нахилені прямі для попереднього та заключного періодів. Їх продовжити вправо та вліво відповідно через середину головного періоду провести пряму, паралельну до вісі ординат, до перетину її з продовженнями попередніх прямих. Відстань між точками перетину відповіда зміні температури при розчиненні солі.
12.Визначивши з графіка Δt1, розрахувати сталу калориметра (К):
![]()
де Qроз- теплота розчинення солі ( -35,62 кДж/моль для KNO3);
m - маса нітрату калію;
М - молярна маса KNO3 (101,1 г/моль );
Δt1- зміна температури при розчиненні солі.
Дослід 2. Визначення теплоти розчинення кристалогідрату (СuSО4•5Н2О)
1. Аналогічно до попереднього досліду зважують близько 5-7 г подрібненого мідного купоросу та вміщують його в пробірку, дані зважування заносять до таблиці 1.
2. Проводять вимірювання у відповідності до п.п. 6-10 попереднього досліду. Результати заносять в таблицю 2; будують графік, за яким визначають зміну температури при розчиненні солі (Δt2)
3. Визначають теплоту розчинення (Q1) солі за формулою:
![]() ,
,
де n - кількість речовини СuSО4•5Н2О.
Дослід 3. Визначення теплоти розчинення безводної солі (СuSО4)
1. Беруть наважку безводного сульфату міді масою 4-5г і проводять дослід аналогічно до попереднього. Дані заносять в таблицю 2. Будують відповідний графік і знаходять зміну температури при розчиненні безводної сол (Δt3).
2. Визначають теплоту розчинення (Q2) солі за формулою:
![]() ,
,
де n - кількість речовини СuSО4.
3. Визначають теплоту утворення кристалогідрату (Q3) з безводно солі:
Q3 = Q2 – Q1
4. Розрахувати відносну похибку експерименту, якщо інтегральна теплота розчинення безводної солі +39,04кДж/моль, а кристалогідрату - рівна -11,72кДж/моль.
5. Результати всіх дослідів занести в таблиці 1 та 2.
6. Зробити відповідні висновки.
Результати роботи:
Дослід 1. Визначення сталої калориметра
1. Розрахунок маси наважки солі KNO3:
Таблиця 1.1
|
Пробірка з сіллю, г |
22,33 |
|
Пуста пробірка, г |
17,50 |
|
Сіль, г |
4,83 |
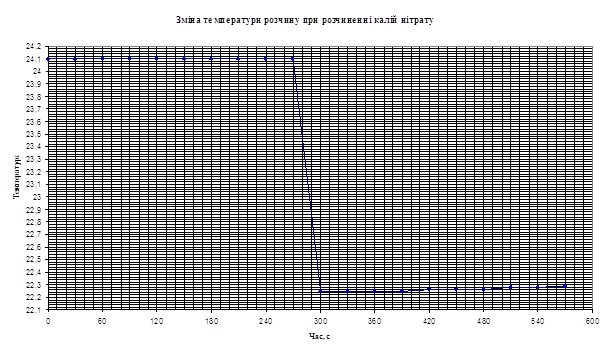
2. Температурн показники для розчину солі KNO3:
Таблиця 1.2
| Температура | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| до розчинення | 24,10 | 24,10 | 24,10 | 24,10 | 24,10 | 24,10 | 24,10 | 24,10 | 24,10 | 24,10 |
| 22,25 | 22,25 | 22,25 | 22,25 | 22,26 | 22,26 | 22,26 | 22,28 | 22,28 | 22,29 |
3. Розрахунок сталої калориметра:
![]()
Дослід 2. Визначення теплоти розчинення кристалогідрату (СuSО4•5Н2О)
1. Розрахунок маси наважки солі СuSО4•5Н2О:
Таблиця 2.1
|
Пробірка з сіллю, г |
23,50 |
|
Пуста пробірка, г |
17,50 |
|
Сіль, г |
6,00 |
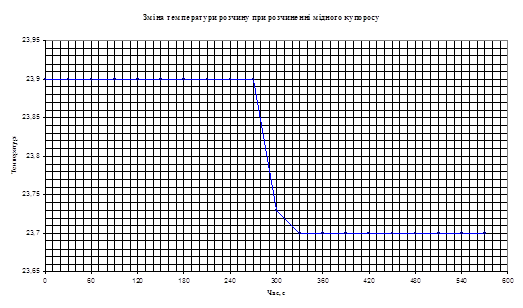
2. Температурн показники для розчину солі СuSО4•5Н2О:
Таблиця 2.2
| Температура | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| до розчинення | 23,90 | 23,90 | 23,90 | 23,90 | 23,90 | 23,90 | 23,90 | 23,90 | 23,90 | 23,90 |
| після розчинення | 23,73 | 23,70 | 23,70 | 23,70 | 23,70 | 23,70 | 23,70 | 23,70 | 23,70 | 23,70 |
3. Розрахунок теплоти гідратації солі СuSО4•5Н2О:
![]() ;
;
![]()
Дослід 3. Визначення теплоти розчинення безводної солі (СuSО4)
1. Розрахунок маси наважки солі СuSО4:
Таблиця 3.1
|
Пробірка з сіллю, г |
22,00 |
|
Пуста пробірка, г |
17,50 |
|
Сіль, г |
4,50 |
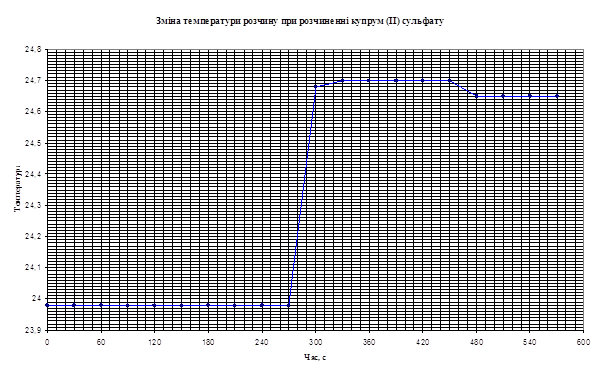
2. Температурн показники для розчину солі СuSО4:
Таблиця 3.2
| Температура | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| до розчинення | 23,98 | 23,98 | 23,98 | 23,98 | 23,98 | 23,98 | 23,98 | 23,98 | 23,98 | 23,98 |
| 24,68 | 24,70 | 24,70 | 24,70 | 24,70 | 24,70 | 24,65 | 24,65 | 24,65 | 24,65 |
3. Розрахунок теплоти гідратації солі СuSО4:
![]() ;
;
![]()
4. Визначення теплоти утворення кристалогідрату з безводної солі:
![]()
5. Розрахунок відносної похибки досліду:
![]()
![]()
![]()
![]()
Висновок:
В процес виконання роботи ми познайомились з калориметричним методом вимірювання теплових ефектів, визначили теплоти розчинення безводного купрум (II) сульфату і мідного купоросу, визначили теплоту утворення кристалогідрату СuSО4•5Н2О з безводної солі.